Представьте себе маленькое терапевтическое устройство, помещённое в кровоток, которое отбирает из него определённые клетки и накапливает их или просто передаёт им некий биохимический сигнал. Неужели опять нанобот? Нет. Перед нами продукт биоинженерии: виртуозная комбинация правильных веществ в правильном месте.
Серийный аппарат, пока не имеющий какого-то особенного названия, проектируется с таким расчётом, чтобы он умел определять в кровотоке целевые клетки (это могут быть клетки иммунной системы, раковые клетки или стволовые клетки) и проводить с ними необходимые манипуляции.
Устройство должно уметь посылать строго отобранным клеткам некие команды (посредством биохимических сигналов), захватывать нужные клетки для последующего использования в другом месте (или для "перепрограммирования"), или даже уничтожать клетки (раковые).
Это удивительное устройство может быть выполнено в виде некоего микроскопического объекта, введённого в сосуд, либо как шунт, через который направляется поток крови. Оно должно помочь медикам в лечении целого ряда заболеваний, или в их диагностике. При этом "клеточный селекционер" должен выпускаться серийно.
Такова смелая цель американской компании CellTraffix, которая и финансирует данное исследование группы учёных. Ключевые фигуры проекта: Майкл Кинг (Michael King) из университета Рочестера (University of Rochester), являющийся также научным консультантом CellTraffix и автором устройства выборочного захвата клеток из кровотока, Джеффри Карп (Jeffrey Karp) из отделения медицинских наук и технологий Гарварда-МТИ (Harvard-MIT Health Sciences and Technology) и Сынпхё Хон (Seungpyo Hong) из Массачусетского технологического института (MIT).
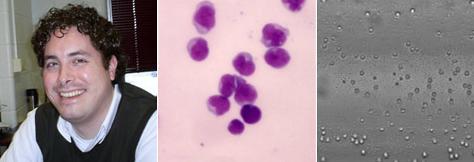 |
Майкл Кинг. Справа: набор снимков, показывающих некоторые из его прошлых опытов по сбору определённых клеток при помощи устройства с покрытием из селектина (фотографии с сайта rochester.edu). |
Что происходит при этом? Тут работает вовсе не физическое трение, а специфические белки, называемые селектины (P— и E-селектины, и другие). Их в определённых ситуациях начинают вырабатывать клетки эпителия, выстилающие стенки сосуда. Селектины содержат молекулярные структуры, комплиментарные структурам на поверхности тех клеток крови, которых эти белки должны вылавливать из кровотока. За счёт химических связей между этими структурами и происходит приклеивание.
| ||
Кинг решил, что если научиться воспроизводить такой захват клеток из потока, можно будет затем делать с этими клетками что потребуется — хоть управлять их работой, хоть просто убивать. Чтобы проверить, как это будет работать, группа Карпа нанесла на поверхность стекла P-селектин и пустила по стеклу раствор с клетками. Как и следовало ожидать, селектин начал вылавливать из потока те клетки, на которые он был рассчитан.
Увы, такое белковое покрытие оставалась стабильным лишь несколько часов, а затем разрушалось. В имплантате же захват клеток должен работать недели и даже месяцы, иначе пациентам придётся постоянно наведываться в госпиталь для замены устройства.
Выход был найден совсем недавно. Оказалось, что хорошую адгезию селектина к стеклу обеспечивает полиэтиленгликоль (PEG). При этом данное вещество не реагирует с другими белками и не захватывает их. Для имплантата – то, что нужно.
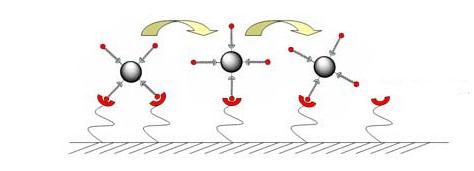 |
Микросферы, снабжённые "лучами" — специфическими молекулами, прокатываются по поверхности устройства, состоящего из подложки (внизу) и закреплённого на ней белка-селектина (красные дуги) (иллюстрация Seungpyo Hong, MIT) |
| ||
Подробности своих опытов учёные изложили в статье в журнале Langmuir.
Следующий шаг исследователей — добавление к связке PEG-селектин терапевтических агентов, взаимодействующих с отобранными клетками.
Таким специфическим агентом, при необходимости, может быть соединение, являющееся для клетки сигналом, который активирует апоптоз – самоубийство клетки. И если устройство захвата будет ловить раковые клетки, распространяющиеся по кровотоку — такой имплантат сможет очищать от них кровь, замедляя или останавливая развитие страшной болезни.
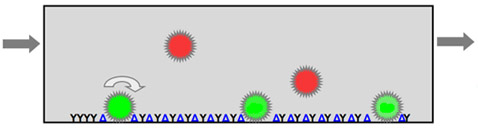 |
Принцип уничтожения раковых клеток (показаны зелёным) новым устройством: селектин (Y), замедляет клетки в кровотоке. Раковые клетки при этом попадают к стенке устройства, где вступают в контакт со специфической молекулой (синий треугольник), включающей в клетке апоптоз, в результате чего та погибает за 2-4 дня. Стрелками показан кровоток и перекатка клеток (иллюстрация с сайта rochester.edu). |
Теперь эту концепцию предстоит проверить в опытах на животных. И первые такие эксперименты, с имплантацией прототипа устройства живым крысам уже выполнены.
Как сообщает CellTraffix, возможность захвата стволовых клеток взрослой особи прямо из её кровотока доказана. А значит, сделан ещё один шаг на пути к появлению новой технологии на рынке и к созданию целого ряда родственных устройств, которые найдут себе работу в медицине и биологических исследованиях.
Статья получена: Membrana.ru











 Противовирусные препараты: за и против
Противовирусные препараты: за и против Добро пожаловать в Армению. Знакомство с Арменией
Добро пожаловать в Армению. Знакомство с Арменией Крыша из сэндвич панелей для индивидуального строительства
Крыша из сэндвич панелей для индивидуального строительства Возможно ли отменить договор купли-продажи квартиры, если он был уже подписан
Возможно ли отменить договор купли-продажи квартиры, если он был уже подписан Как выбрать блеск для губ
Как выбрать блеск для губ Чего боятся мужчины
Чего боятся мужчины Как побороть страх перед неизвестностью
Как побороть страх перед неизвестностью Газон на участке своими руками
Газон на участке своими руками Как правильно стирать шторы
Как правильно стирать шторы Как просто бросить курить
Как просто бросить курить

 - 2037 -
- 2037 -


