Почти будничными стали сообщения о создании физиками каких-нибудь мудрёных наноструктур — то "деревьев", то "цветов". Но вот, оказывается, и сама природа может стать конструктором, преподнеся исследователем "на блюдечке" почти готовое наноустройство. Бери и пользуйся.
Это открытие было сделано случайно. Нынешней весной учёные из американской лаборатории Беркли (Berkeley Lab) проводили опыты с нанокристаллами кобальта (шарики, насчитывающие лишь несколько тысяч атомов) и поместили их как-то в серу.
На первый взгляд, результат был ожидаемый — образовались шарики сульфида кобальта.
Но вот рассмотрев их под электронным микроскопом внимательнее, учёные удивились — это были не шары, а полые сферы.
Ядун Инь (Yadong Yin), ведущий исследование, собрал коллег, и начался мозговой штурм.
В результате решили, что виновником чудесного превращения является эффект Эрнеста Киркендалла (Ernest Kirkendall), открытый в 1947 году, правда работающий здесь не совсем так, как обычно.
А обычно это выглядит так. Соединяют вместе два взаимодействующих твёрдых материала. Например, два цилиндрика из цинка и меди.
| ||
На границы материалов формируется слой сплава — латуни. Он растёт, но та его граница, что обращена к меди, растёт быстрее.
Казалось бы, и что с того? Оказывается, в таком случае в материале, диффузия которого идёт быстрее (цинк), образуются поры, которые растут и объединяются. Это и есть эффект Киркендалла.
Происходящее с кобальтом и серой подчинялось тому же правилу. Атомы кобальта смещались к месту встречи живее, чем атомы серы. Только разворачивались эти события на сферическом фронте и в наномасштабе. Поры внутри кристалла кобальта, покрытого сначала серой, а затем — сульфидом кобальта, вырастали так, что оставалось лишь ядро в центре, связанное с оболочкой тонкими мостиками убегающих молекул.
Потом исчезали и ядро, и мостики, оставляя идеальную сферу с пустотой внутри.
Учёные попробовали повторить процесс с другими парами материалов: кобальт и кислород, железо и кислород, кадмий и сера… Всё повторялось в точности.
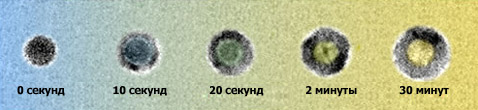 |
Последовательность образования полых наносфер из сульфида кобальта на снимках с электронного микроскопа (фото с сайта lbl.gov). |
Замечательным было и то, что в этом природном производственном процессе сферы получались почти одинаковыми — внутренние пустоты отличались по диаметру не более, чем на 13%.
Тут уж у американских физиков разыгралась фантазия. Таким идеальным сферам нанометрового масштаба можно найти массу применений.
Внутрь можно помещать лекарственные препараты для постепенного выпуска в теле пациента, в оптике и электронике также найдётся, что сделать с такими объектами, а уж химия… Готовый химический реактор, наноколба — разве это не здорово?
При этом для массовой технологии важно, что весь процесс идёт "в одном горшке" — добавил ингредиенты — получил наносферы. Никакого переноса материалов по разным плошкам, никаких потерь. Всё просто.
 |
Схема убегания атомов кобальта по мостикам — с ядра на внешнюю оболочку (иллюстрация с сайта lbl.gov). |
На клич "Посмотрите, что у нас получилось!" прибежали коллеги из других лабораторий и отделов. Химик Габор Соморджей (Gabor Somorjai) предложил: попробуйте поместить внутрь сферы ядро из другого материала, например — платины. Пусть это будет микрореактор с катализатором.
Но как поместить платину в закрытую со всех сторон сферу, дверцы-то нет?
Придумали многостадийный процесс. Сначала брали зёрна платины. Добавляли наночастицы кобальта, формируя ровную сферу вокруг ядра. Потом — кислород. Далее всё происходило по знакомому сценарию.
Через некоторое время весь кобальт реагировал с кислородом и убегал наружу, образовывая оксидную "скорлупу ореха", внутри которой свободно бултыхалось платиновое "ядрышко".
Выяснилось, что такой микрореактор, действуя как катализатор, снижает вероятность побочных реакций, повышая выход целевого продукта, по сравнению с платиной, работающей на открытом пространстве — на плоской поверхности или на поверхности пористых губок (как обычно и делаются устройства-катализаторы).
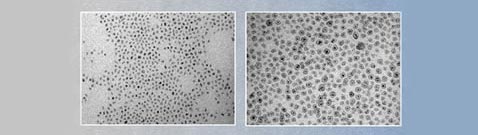 |
Исходные ядрышки платины и они же — в скорлупе из оксида кобальта (фото с сайта lbl.gov). |
Попробовали применить "орехи", как катализаторы в реакции этилена с водородом, и увидели: скрытая платина самым наилучшим образом ускоряла образование этана.
То, что выглядело бы абсурдом в макромасштабе (представьте закрытый сосуд с платиной и исходные продукты снаружи), на наноуровне прекрасно работало.
Однако, как исходные компоненты проникали внутрь "скорлупы" и, как продукт реакции — этан — попадал наружу, осталось пока тайной. Природа-изобретательница не пожелала раскрыть этот патент.
Статья получена: Membrana.ru











 Противовирусные препараты: за и против
Противовирусные препараты: за и против Добро пожаловать в Армению. Знакомство с Арменией
Добро пожаловать в Армению. Знакомство с Арменией Крыша из сэндвич панелей для индивидуального строительства
Крыша из сэндвич панелей для индивидуального строительства Возможно ли отменить договор купли-продажи квартиры, если он был уже подписан
Возможно ли отменить договор купли-продажи квартиры, если он был уже подписан Как выбрать блеск для губ
Как выбрать блеск для губ Чего боятся мужчины
Чего боятся мужчины Как побороть страх перед неизвестностью
Как побороть страх перед неизвестностью Газон на участке своими руками
Газон на участке своими руками Как правильно стирать шторы
Как правильно стирать шторы Как просто бросить курить
Как просто бросить курить

 - 3065 -
- 3065 -



